REVIEW - RỐI LOẠN LIPID MÁU
– KẺ GIẾT NGƯỜI THẦM LẶNG
I – ĐẠI CƯƠNG
Bệnh tim mạch là nguyên nhân gây tử vong hàng đầu ở Việt Nam, cướp đi sinh mạng của 170.000 người hàng năm. Bệnh tim mạch có liên quan đến nhiều yếu tố nguy cơ có thể điều chỉnh được trong y văn, đặc biệt là huyết áp, lipoprotein tỷ trọng thấp (LDL), lipoprotein tỷ trọng cao (HDL), không dung nạp glucose và hút thuốc lá.
Cholesterol toàn phần cao, liên quan đến LDL, HDL và Triglyceride, được coi là cao khi  240 mg/dL. Mức HDL thấp khi ít hơn 40 mg/dL. Với mức LDL mục tiêu dưới 100 mg / dL, 71 triệu (33,5%) người trưởng thành Hoa Kỳ có mức LDL cao với chỉ 23 triệu (33%) trong số này được kiểm soát mức LDL.
240 mg/dL. Mức HDL thấp khi ít hơn 40 mg/dL. Với mức LDL mục tiêu dưới 100 mg / dL, 71 triệu (33,5%) người trưởng thành Hoa Kỳ có mức LDL cao với chỉ 23 triệu (33%) trong số này được kiểm soát mức LDL.
Việc kiểm soát nồng độ cholesterol tăng cao ở người trưởng thành ngày càng quan trọng để giảm tỷ lệ mắc bệnh tim mạch và tỷ lệ biến cố mạch vành. Trong bài này, chúng tôi sẽ xem xét hướng dẫn năm 2018 của Trường Môn Tim mạch Hoa Kỳ/Hiệp hội Tim mạch Hoa Kỳ (ACC / AHA) và update năm 2019. Các loại thuốc mới đang được phát triển để giảm cholesterol kể từ năm 2018.
II – CƠ CHẾ BỆNH SINH
Rối loạn lipid máu liên quan đến lâm sàng tăng nồng độ cholesterol /hoặc Triglyceride có thể đi kèm với giảm mức HDL. Đa số những bệnh nhân này có tăng sản xuất VLDL ở gan liên quan đến nồng độ Triglyceride (TG) tăng cao, giảm HDL cholesterol và tăng LDL cholesterol. Sản xuất quá nhiều VLDL ở gan có thể do yếu tố di truyền, chế độ ăn nhiều carbohydrate, sử dụng rượu quá mức, béo phì, kháng insulin và hội chứng thận hư. Mức độ LDL có quan hệ nhân quả với nguy cơ bệnh tim mạch do xơ vữa động mạch (ASCVD) thông qua nồng độ tuyệt đối và thời gian tích lũy của phơi nhiễm LDL-C. Hiện tại không có bằng chứng cho vai trò bảo vệ của HDL chống lại tình trạng xơ vữa động mạch.
LDL và HDL là những chất vận chuyển lipoprotein chính của các este cholesterol nội sinh; tuy nhiên, chúng cũng mang ít Triglyceride, phospholipid và vitamin tan trong chất béo. Lớp vỏ lipid của lipoprotein chứa apolipoprotein có một số chức năng, bao gồm đóng vai trò như điểm gắn (ligand) cho các thụ thể, đồng yếu tố (cofactors) cho các enzym và cung cấp cấu trúc cơ bản cho lipoprotein. Các apolipoprotein LDL bao gồm ApoB-100 và các apolipoprotein HDL bao gồm ApoAI, ApoA-II, ApoA-IV, ApoA-V, ApoC-III và ApoE. Bản thân lipoprotein có nhiệm vụ vận chuyển lipid có trong chế độ ăn uống và lipid sản xuất từ gan đi khắp cơ thể đến các mô cần năng lượng hoặc dự trữ axit béo. Ví dụ, HDL dùng để vận chuyển cholesterol từ các tế bào ngoại vi đến gan và ruột. HDL vận chuyển cholesterol ngoại vi đến gan thông qua thụ thể xác định lớp B1 và trao đổi các este cholesterol chứa TG từ các tế bào LDL thông qua cholesteryl ester transfer protein. Các este cholesterol được chuyển đến các hạt LDL sau đó có thể được loại bỏ khỏi tuần hoàn thông qua quá trình nhập bào qua trung gian thụ thể LDL ở gan. Sau đó, cholesterol có thể được thủy phân và bài tiết vào mật.
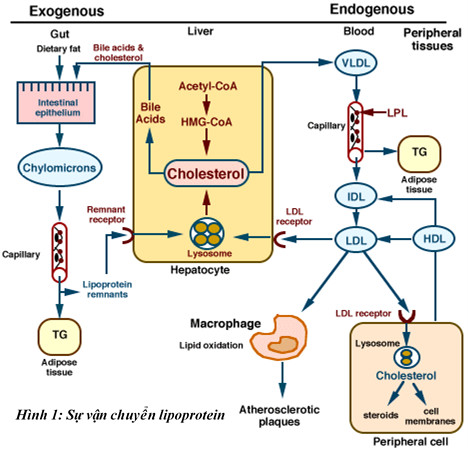
Cholesterol trong cơ thể tăng cao có thể dẫn đến sự hình thành và tích tụ mảng bám trong mạch máu, dẫn đến bệnh tim mạch do xơ vữa như tóm tắt trong Hình 2. Ba giai đoạn sinh bệnh của xơ vữa động mạch là khởi phát, tiến triển và biến chứng. Cholesterol LDL đóng một vai trò lớn trong giai đoạn khởi đầu.
Các hạt LDL có thể xâm nhập qua lớp nội mạc mạch máu bị rối loạn chức năng và gây ra tình trạng viêm sau đó. Khả năng lưu giữ LDL nội mạc bị ảnh hưởng bởi kiểu hình nội mô và nồng độ LDL huyết thanh. Yếu tố phiên mã Krupper-like Factor 2 (KLF2) có liên quan đến huyết động học bảo vệ động mạch. KLF2 thúc đẩy hoạt động kháng viêm, chống huyết khối và tạo xơ vữa ở nội mạc thông qua con đường tín hiệu MEK5/MEF2, làm giảm tính nhạy cảm của nội mạc mạch máu với các hạt LDL xâm lấn gây xơ vữa động mạch. Thuốc ức chế HMG-CoA reductase, được sử dụng rộng rãi trong điều trị tăng cholesterol máu, cũng đã được phát hiện có khả năng điều chỉnh biểu hiện KLF2 có thể góp phần vào tác dụng bảo vệ tim mạch của nhóm thuốc này. Khả năng LDL xâm nhập vào nội mô bị rối loạn chức năng cũng phụ thuộc vào nồng độ LDL trong huyết thanh. Khi LDL-C cao hơn 20-40 mg/dL, có sự gia tăng phụ thuộc nồng độ trong khả năng xâm lấn nội bộ của LDL và tiến triển thành xơ vữa động mạch.
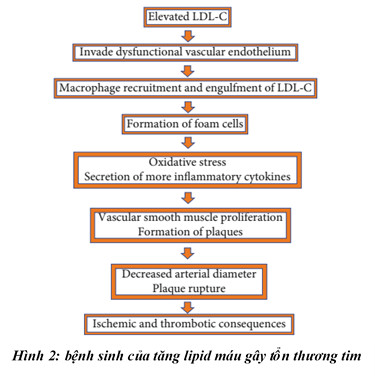 Sau khi các hạt LDL xâm nhập vào lớp nội mạc bị rối loạn chức năng, các phân tử lipid có thể bị thay đổi, ôxy hóa hoặc glycosyl hóa thành các hạt LDL biến đổi. Các hạt LDL trong nội mô cũng có thể liên kết với các proteoglycan để tập hợp lại với nhau và xâm nhập vào các tế bào cơ trơn, dẫn đến tích tụ lipid nhiều hơn. Để đáp ứng với sự xâm nhập LDL vào nội mô, bạch cầu đơn nhân xâm nhập vào khoảng dưới nội mô. Các đại thực bào hấp thu các hạt LDL biến đổi và trở thành các tế bào bọt (foam cell), do lượng cholesterol cao của chúng. Các tế bào bọt này gây ra stress oxy hóa và tiết ra các cytokine liên quan đến sự phát triển của mảng bám, và cái chết của chúng có thể thúc đẩy quá trình viêm, dẫn đến tăng sinh cơ trơn mạch máu và hình thành các mảng xơ vữa. Các nghiên cứu gần đây cho thấy rằng tế bào cơ trơn chuyển sản thành các tế bào bọt giống như đại thực bào. Trong khi các đại thực bào đơn nhân chiếm phần lớn các tế bào bọt, sự di chuyển của tế bào cơ trơn từ lớp media đến lớp nội mô góp phần làm mảng bám mở rộng. Quá trình hình thành mảng xơ vữa động mạch có thể dẫn đến giảm đường kính động mạch và vỡ mảng bám, có khả năng gây ra hậu quả thiếu máu cục bộ hoặc huyết khối.
Sau khi các hạt LDL xâm nhập vào lớp nội mạc bị rối loạn chức năng, các phân tử lipid có thể bị thay đổi, ôxy hóa hoặc glycosyl hóa thành các hạt LDL biến đổi. Các hạt LDL trong nội mô cũng có thể liên kết với các proteoglycan để tập hợp lại với nhau và xâm nhập vào các tế bào cơ trơn, dẫn đến tích tụ lipid nhiều hơn. Để đáp ứng với sự xâm nhập LDL vào nội mô, bạch cầu đơn nhân xâm nhập vào khoảng dưới nội mô. Các đại thực bào hấp thu các hạt LDL biến đổi và trở thành các tế bào bọt (foam cell), do lượng cholesterol cao của chúng. Các tế bào bọt này gây ra stress oxy hóa và tiết ra các cytokine liên quan đến sự phát triển của mảng bám, và cái chết của chúng có thể thúc đẩy quá trình viêm, dẫn đến tăng sinh cơ trơn mạch máu và hình thành các mảng xơ vữa. Các nghiên cứu gần đây cho thấy rằng tế bào cơ trơn chuyển sản thành các tế bào bọt giống như đại thực bào. Trong khi các đại thực bào đơn nhân chiếm phần lớn các tế bào bọt, sự di chuyển của tế bào cơ trơn từ lớp media đến lớp nội mô góp phần làm mảng bám mở rộng. Quá trình hình thành mảng xơ vữa động mạch có thể dẫn đến giảm đường kính động mạch và vỡ mảng bám, có khả năng gây ra hậu quả thiếu máu cục bộ hoặc huyết khối.
Thuốc hạ lipid máu đã được chứng minh là có hiệu quả trong việc giảm nguy cơ mắc bệnh tim mạch do xơ vữa động mạch, làm nổi bật mối liên hệ nhân quả giữa rối loạn lipid máu và xơ vữa động mạch. Statin, chất ức chế HMG-CoA reductase, làm giảm nồng độ LDL-C trong huyết tương. Một phân tích tổng hợp đã chứng minh việc giảm nguy cơ mắc các biến cố tim mạch chính theo liều lượng tỷ lệ thuận với việc giảm LDL-C từ việc điều trị. Ezetimibe ức chế sự hấp thu cholesterol ở ruột, trong đó liệu pháp ezetimibe có liên quan đến việc giảm tỷ lệ các biến cố tim mạch. Kháng thể đơn dòng PCSK9 làm tăng độ thanh thải LDL khỏi máu và có liên quan đến việc giảm nguy cơ biến cố tim mạch. Do đó, các phương pháp điều trị rối loạn lipid máu làm giảm nồng độ lipid có thể ảnh hưởng lớn đến kết quả tim mạch của những bệnh nhân này.
III – ĐẶC ĐIỂM LÂM SÀNG
Tăng cholesterol máu thường không có triệu chứng rõ ràng nhưng là một yếu tố nguy cơ chính của bệnh tim mạch. Mức cholesterol rất cao (very high), thường thấy trong tăng cholesterol máu gia đình, có thể biểu hiện thành xanthomas và viêm giác mạc. Các biến chứng do tăng cholesterol máu không được điều trị bao gồm bệnh động mạch cảnh, đột quỵ, bệnh mạch máu ngoại vi, huyết áp cao và bệnh đái tháo đường type 2 (T2DM).
Các bệnh hệ thống liên quan đến ảnh hưởng đến rối loạn lipid máu bao gồm bệnh vẩy nến, bệnh Crohn’s, bệnh viêm ruột, bệnh phổi tắc nghẽn mãn tính, trầm cảm, đau mãn tính và bệnh thận mạn. Các biến chứng do tăng cholesterol máu có thể được kiểm soát thông qua điểu trị tối ưu. Có nhiều hướng dẫn về việc sử dụng các loại thuốc hạ lipid đang được phát triển để giúp giảm cholesterol. Trong bài này, chúng tôi sẽ tóm tắt hướng dẫn ACC/AHA 2018 và đánh giá các loại thuốc mới đã được phát triển kể từ khi ban hành hướng dẫn năm 2018.
IV – HƯỚNG DẪN ACC/AHA 2018
Các bản cập nhật khác đối với các hướng dẫn về lipid năm 2013 cho đến khi ACC/AHA ra mắt với Hướng dẫn về Quản lý Cholesterol trong máu năm 2018. Nó thừa nhận rằng mặc dù không có mức LDL-C mục tiêu lý tưởng, nhưng điều quan trọng nhất là giữ cho mức đó ở mức thấp, vì người trưởng thành có mức LDL-C bằng hoặc dưới 100 mg/dL ít có nguy cơ mắc bệnh tim và đột quỵ. Ngoài việc kiểm tra các yếu tố nguy cơ thường liên quan đến bệnh tim mạch như cholesterol cao, tăng huyết áp và hút thuốc lá, hướng dẫn năm 2018 cũng khuyến cáo xem xét các yếu tố tăng nguy cơ ở bệnh nhân lớn tuổi từ 40 đến 75, bao gồm tiền sử gia đình và các yếu tố tình trạng sức khỏe khác. Bằng cách đó, nó cung cấp một bản mô tả về nguy cơ cá thể hóa hơn cho bệnh nhân. Một bổ sung quan trọng khác của hướng dẫn năm 2018 là việc sử dụng thang điểm canxi động mạch vành (coronary artery calcium - CAC) được sử dụng để phân loại lại những bệnh nhân có nguy cơ ở mức giới hạn hoặc nguy cơ trung bình, những người mà nguy cơ điều trị bằng statin là không chắc chắn.
Về điều trị tăng cholesterol, thay đổi lối sống như giảm lượng chất béo bão hòa và tập thể dục ít nhất 40 phút, 3 đến 4 lần một tuần thường là bước đầu tiên trong điều trị, trừ khi bệnh nhân có nguy cơ mắc ASCVD rất cao.
Hướng dẫn năm 2018 không chỉ cho phép chăm sóc cá thể hóa hơn và nhiều lựa chọn điều trị hơn với việc giới thiệu các liệu pháp non-statin như ezetimibe và chất hấp phụ axit mật, mà còn bao gồm các chiến lược đánh giá rủi ro bổ sung để ngăn chặn việc kê đơn điều trị statin không cần thiết.
V – CÁC THUỐC MỚI TỪ NĂM 2018
Kể từ khi hướng dẫn hạ lipid máu năm 2018 được ban hành, đã có vô số loại thuốc hạ lipid mới hiện đang được nghiên cứu thử nghiệm rộng rãi với hy vọng có khả năng được đưa ra thị trường trong tương lai gần.
Inclisiran có thể là phương pháp điều trị siRNA giảm LDL-C đầu tiên và duy nhất. Nó được tiêm dưới da với liều ban đầu, liều thứ hai sau 3 tháng, và sau đó, cứ sáu tháng một lần. Bằng cách tăng tái sử dụng và biểu hiện thụ thể LDL-C trên bề mặt tế bào gan, Inclisiran do đó làm tăng sự hấp thu LDL-C của tế bào gan và làm giảm mức LDL-C trong máu.
Evinacumab ức chế angiopoietin-like 3 (ANGPTL3), bản thân nó là chất ức chế lipoprotein và lipase nội mô có trách nhiệm làm tăng mức triglyceride và các lipid khác. Vì đột biến mất chức năng ANGPTL3 thường liên quan đến mức LDL-C thấp hơn độc lập với thụ thể LDL, cơ chế hoạt động của Evinacumab cố gắng đạt được kết quả tương tự. Vupanorsen (AKCEA-ANGPTL3) làm giảm sản xuất protein ANGPTL3, cuối cùng dẫn đến giảm mức LDL-C. Ngoài việc giảm phụ thuộc liều ANGPTL3 và LDL-C, Vupanorsen cũng cho thấy làm giảm TG, non -HDL-C và cholesterol toàn phần. Gemcabene có thể tăng cường thanh thải VLDL trong huyết tương, ức chế sản xuất cholesterol và TGs trong gan thông qua việc điều hòa giảm apolipoprotein C-III ở gan (apoC-III). ARO-ANG3 cũng ức chế ANGPTL3 và được thiết kế để làm giảm Triglyceride và giảm LDL-C ở bệnh nhân rối loạn lipid máu hỗn hợp. Axit bempedoic ức chế ATP-citrate lyase, là một thành phần của con đường tổng hợp cholesterol.
.jpg)
VI – KẾT LUẬN
Khi truyền thông bệnh nhân về tăng cholesterol, thường không phải đề cập đến cholesterol toàn phần mà là mức LDL thực tế. Đôi khi được gọi là "cholesterol xấu". Mức LDL lý tưởng nên dưới 100 mg/dL; tuy nhiên ở những người bị bệnh tim mạch hoặc đái tháo đường, mức tối ưu phải dưới 70 mg/dL hoặc giảm ít nhất 50%. Việc sử dụng liệu pháp statin là yếu tố then chốt trong việc đạt được mức LDL tối ưu, đặc biệt quan trọng ở bốn nhóm nguy cơ cao: (1) bệnh nhân có nguy cơ ASCVD lớn hơn 7,5%, (2) những người có tiền sử tăng cholesterol máu gia đình, (3) bệnh nhân có tiền sử bệnh xơ vữa động mạch, và (4) bệnh nhân đái tháo đường. Statin liều cao cũng như tuân thủ chế độ ăn uống và điều chỉnh lối sống đã được chứng minh là có hiệu quả trong việc ngăn ngừa các biến cố mạch vành. Tuy nhiên, với sự ra đời của các loại thuốc mới hơn, có khả năng thay thế statin.

Ý kiến bạn đọc